
基于GMR传感器阵列的生物检测研究
0 引 言
生物传感器的研究具有巨大的应用前景,近年来,随着电子自旋现象的发现,结合了半导体微电子工艺制备的GMR设备,在生物检测领域引起了人们越来越浓厚的研究兴趣,使其成为传统生物检测方法的替换方案之一。由于其独特的物理特性,GMR传感器比电子传感器更灵敏、可重复性强,具有更宽的工作温度、工作电压和抗机械冲击、震动的优异性能,而且GMR传感器的工作点也不会随时间推移而发生偏移。GMR传感器的制备成本和检测成本低,对样本的需求量很小。由GMR传感器组成的阵列,还可以结合现有的IC工艺,提高整体设备的集成度,进行多目标的检测。同时,对比传统的荧光检测法,磁性标记没有很强的环境噪声,标记本身不会逐渐消退,也不需要昂贵的光学扫描设备以及专业的 *** 作人员。因此,无论是传感器本身的性能,还是磁性标记的特点,都决定了GMR传感器阵列在生物检测领域的研究具有较高的应用价值和实践意义。
1 巨磁阻阵列传感器生物检测的基本原理
1.1 巨磁阻(GMR)效应
1988年派瑞松大学的研究人员发现了GMR效应,这是一种在铁磁性层与非铁磁性层交替叠置的结构中观测到的量子效应,是指某些磁性或合金材料的磁电阻在一定磁场作用下急剧减小,而△ρ/ρ急剧增大的特性,一般增大的幅度比通常的磁性与合金材料的磁电阻约高10倍。GMR效应的理论很复杂,许多机理至今还不清楚,目前普遍接受的解释是两流模型,如图1所示。多个铁磁层中的磁矩方向由施加的外磁场控制,当铁磁性层的磁矩反平行排列时见图1(a),载流子受到的自旋散射最大,多层膜电阻最高;当铁磁性层的磁矩平行排列时见图1(b),载流子受到的自旋散射最小,多层膜的电阻最低。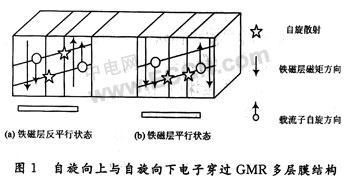
目前,按其结构、GMR材料可分为具有层间偶合特性的多层膜(例如Fe/Cr)、自旋阀多层膜(例如FeMn/FeNi/Cu/FeNi)、颗粒型多层膜(例如Fe-Co)和钙钛矿氧化物型多层膜(例如AMnO3)等。
1.2 巨磁阻(GMR)的电子特性
图2是一个典型的多层GMR材料在外加磁场下的电阻变化情况。图2中的输出表明,无论是正向还是反向的外加磁场变化,都能带来相同的磁阻变化,也就是说GMR效应是全极性的。曲线的斜率体现了磁性敏感程度,通常以V(mV)/Oe为单位。当阻值不随磁场继续变化时,磁性材料就达到了其磁性饱和区。两条曲线中的偏移是磁性材料的磁滞导致的,从零磁场到饱和磁场所带来的阻值变化就称为磁阻。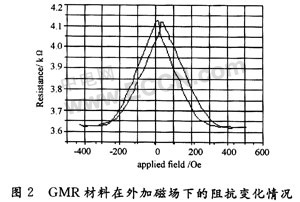
1.3 GMR阵列传感器生物检测的基本模式
用GMR阵列传感器进行生物检测,是以磁性颗粒为标记物,采用直接标记法或两步标记法,在施加一定方向的外加磁场的情况下,用磁敏传感器对磁性标记产生的寄生磁场进行检测,从而实现对生物目标定性定量分析。图3分别介绍了磁性标记法检测的具体步骤: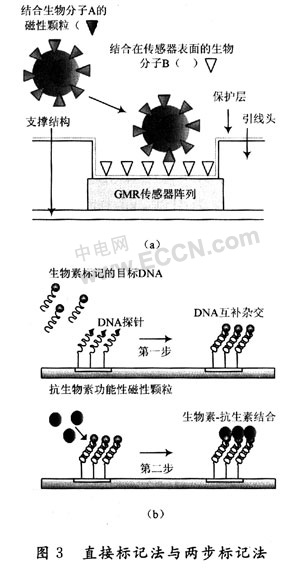
直接标记法 如图3(a)所示,直接标记法是将标记物直接结合到探针上。首先在传感器表面结合特定的生物探针,再将已预先绑定磁性颗粒的样本溶液加入传感器的反应池中,溶液中特定的目标分子被探针捕获,完成标记。
两步标记法 如图3(b)所示,以DNA检测为例,第一步将已知序列的DNA探针链结合在包埋了自旋阀传感器的芯片表面,加入用生物素标记的DNA目标链溶液,进行充分杂交;第二步,加入被抗生物素包裹的磁性颗粒,形成生物素一抗生物素共价键,从而选择性地捕获磁性标记。
标记反应完成后,用外加梯度磁场将未参与标记的多余磁性颗粒分离,再施加激励磁场将磁标记(磁性颗粒)磁化,磁化的磁标记产生的寄生磁场引起传感器阻值的变化,从而导致反映生物反应的信号输出。
2 GMR生物检测系统设计
当前,国际国内已经开展了基于不同技术的生物磁场检测设备研究,涉及自旋阀传感器(Spin Valves)、感应传感器(InducTIve Sensors)、超导量子干涉仪(SQUIDs)、各向异性磁阻(AMR)环式传感器、小规模的霍耳组合传感器(Hall Crosses)以及隧道结(TMR)传感器等。
1998年,作为美国国防部高级研究规划局(DAR-PA)支持项目,美国海军研究实验室与NVE公司合作,由David R.Baselt等开展了基于巨磁阻技术的生物传感器研究,并设计制备了两代GMR传感器的磁珠阵列计数器(BARCⅡ,BARCⅢ)进行生物杂交分析,并用于测量在单个分子水平上的DNA-DNA,以及抗体抗原对和受体-配体对的结合力。德国比勒菲尔德(Bielefeld)大学、美国佛罗里达州立大学、美国斯坦福大学、葡萄牙国立计算机系统与工程研究所(INESC-MN)等研究机构也相继开展了磁性传感器阵列的生物检测研究。国内多所高校和研究所,如中科院物理研究所、清华大学、同济大学、电子科技大学、中山大学等,自2005年起,对巨磁阻生物传感器阵列设计、传感器材料的选取、磁性标记与传感器尺寸关系、输出信号处理等方面进行了广泛的研究,实现了单个纳米尺度颗粒的检测,并申请了相关的专利。
上述研究中采用的阵列方案和传感器形态各异,从布局上可以类分为规则排列阵列或分区排列阵列;矩形传感器或蛇形传感器。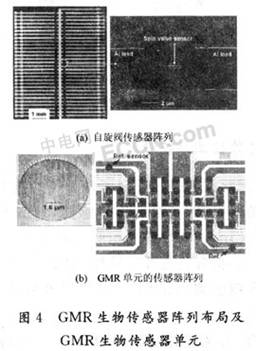
图4(a)是Glaanxiong Li等在约7 mm×8 mm的芯片表面上制备的自旋阀传感器阵列,阵列包含60个亚微米级的条形自旋阀传感器,呈2个纵列排列,每列30个传感器单元,每个单元两头通过ion束沉积厚约300 nm的铝作为引线,而中间未被覆盖的条形区域作为生物反应区,用于感应与其易轴同向的磁场分量。
图4(b)是David R.Baselt等设计制备的含66个GMR单元的传感器阵列(BARCⅢ),分为8个反应区,每区8个单元,可进行多路检测。其单元呈圆形,直径为200 μm,由长8 mm宽1.6μm的电阻蛇形蜿蜒而成。
通常,整个GMR生物检测系统由微流部分、GMR阵列、驱动部分、分析处理部分组成。为了减少外界环境对传感器输出稳定性的影响,传感器单元往往与参考单元一起组成惠斯通电桥。如图5所示,GMR电阻对组成惠斯通半桥,其中一个电阻表面覆盖软磁性屏蔽层,不受外加磁场的影响;另一个电阻作为应变电阻,在GMR效应作用下,阻值随外加磁场变化,导致电桥输出微伏级的差分电压值,输出的电压经过过滤、放大等处理后,再输送到后端的采集检测设备,做进一步分析。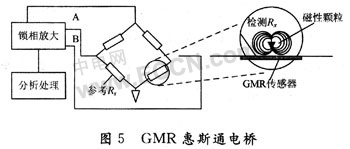
3 系统性能分析与讨论
Darid R.Baselt等1998年研制的GMR生物传感器,由于信噪比的限制,只能实现在每80 μm×5 μm的区域上探测到一个磁珠(直径为2.8 μm);2002年,Schotter等人实现了对低磁珠密度(16 pg/μl)被测样品的探测;2005年,INESC公司采用U型自旋阀结构制作GMR生物传感器,其工作频率从传统的200 Hz降低到了30 Hz,使得热噪声更低(10-17/2V/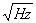 );2005年,加利福尼亚大学物理系D.K.Wood等人研制的亚微型新一代GMR生物传感器,可实现对小尺寸磁珠(直径200 nm)的探测,且灵敏度更高(2×10-16emu/
);2005年,加利福尼亚大学物理系D.K.Wood等人研制的亚微型新一代GMR生物传感器,可实现对小尺寸磁珠(直径200 nm)的探测,且灵敏度更高(2×10-16emu/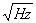 )。虽然磁性生物检测系统取得一定的成绩,但距离实用化仍有很大的距离。
)。虽然磁性生物检测系统取得一定的成绩,但距离实用化仍有很大的距离。
综合现有技术,提高磁性生物检测系统的性能,可以在传感器特性、磁性颗粒的选择以及外围电路的设计等方面进行改进。
3.1传感器灵敏度
GMR传感器灵敏度是指其对微弱信号的感应能力。由于磁性标记体积非常小,所以产生的寄生磁场也非常微弱,因此必须选用灵敏度高的磁性材料制备传感器。衡量GMR性能的两个最基本参数是:
(1)在一定温度下所能达到的最大GMR值;
(2)获得最大GMR效应所需施加的饱和外磁场强度。
在各种巨磁电阻材料中,多层膜和颗粒膜饱和磁场高达数特斯拉,其磁场灵敏度低;氧化物陶瓷类材料饱和场极高,难以实现实用化;自旋阀材料饱和磁场较低,仅为几个或几十奥斯特,但室温下GMR不高。因此,寻求GMR值高,饱和磁场低,磁场灵敏度高的合金体系或人工薄膜结构是GMR传感器生物检测实用化的难点和重点。
目前,从制作的难易程度、性能的稳定性等方面来考虑,传感器阵列多采用GMR多层膜耦合结构和自旋阀结构,随着研究工作的逐步深入,将来具有更高磁阻率的结构,如隧穿磁阻(TMR)、稀土氧化物、微晶或非晶软磁合金薄膜,以及利用巨磁阻抗效应(GMI)的高灵敏传感器,将在磁性生物阵列检测中得以应用。
3.2磁性微粒的尺寸与磁性含量
在整个系统中,生物特异性反应通过磁性微粒的存在与数量来体现。目前采用的磁性颗粒(如γ-Fe2O3,Fe3Ot,NiFe等)可分为微米级和亚微米级两类,较大的磁性颗粒(约1~3μm)在形状上比较容易实现统一,虽然磁性物质含量较低(约15%),但相对较大的体积,磁性微粒在传感器表面产生的磁场分量仍然较大,另外,大体积也便于显微计数。其缺点是无法高密度地绑定在传感器表面,因此检测到的生物分子较少。纳米尺度的磁性颗粒具有很高的磁性含量(70%~80%),但是由于制备工艺的限制,同一批次,其大小和形状都有较大差异,对定量分析非常不利。而且,体积小的纳米磁性颗粒容易快速簇集,导致输出的信号失真。但是,采用敏感度更高的传感器和更先进的检测分析系统,可以部分满足小体积磁性颗粒的应用要求,2005年,美国斯坦福大学Guanxiong Li等实验验证了当自旋阀传感器阵列尺寸与磁性颗粒尺寸(直径为16 nm的超顺磁Fe3O4颗粒)相近时,传感器输出信号与绑定的颗粒数量呈比较理想的正比关系,从而体现了采用小体积纳米磁性标记,自旋阀传感器阵列在生物检测中的定量分析能力。
3.3传感器阵列的物理参数
GMR传感器合适的层厚可以保证两个磁性层反平行耦合,从而保证在没有外加磁场的情况下,设备处于高电阻值状态。另外,因为GMR传感器的电阻值主要取决于电子自旋散射,所以其层厚必须比大部分材料中电子的平均自由程(约几个纳米)小,典型的GMR磁性传感器的层厚大约是2~6 nm。
同时,采用与生物分子尺度相同的传感器(蛋白质、DNA、RNA和病毒等都在1~100 nm的尺度范围),能够有效增加检测的灵敏度。目前,受制于制备的复杂性,减小传感器的尺寸仍然十分困难,国内研究机构应用传统的光学光刻技术,受光波波长和数值孔径等因素的限制,难以制作线宽小于100 nm的图案。然而更先进的极端远紫外光刻、电子束直写、离子投影光刻技术、X光光刻、电子束投影等技术虽然能克服上述限制,但系统复杂,造价十分昂贵。因而,基于传统光刻技术上改进的浸没式光刻系统、微接触印刷、纳米压印光刻等新的制备技术,将是基材表面批量获取纳米量级GMR传感器阵列中最具潜力的技术。
除传感器本身的物理参数外,GMR传感器对磁场的距离也非常敏感,磁性颗粒的寄生磁场随其与传感器敏感层的距离呈3阶衰减,所以,应尽量减小传感器与磁性标记之间的距离,以减少对传感器灵敏度的过高要求。但是,在实际检测中,为了防止传感器表面被生物溶液侵蚀和牢固结合生物探针,又必须在传感器表面覆盖保护层(7 nm PEI/PMMA;1 μm氮化硅)和生物结合层(金属材料、玻璃、石英或表面为氧化硅的硅片)。因此,超薄惰性材料和生物结合材料的发现与工艺的提高也是提高磁性生物检测系统性能必不可少的条件。
3.4外加磁场
检测中需要外加激励磁场磁化超顺磁颗粒,针对不同的磁性传感器,磁性激励场可以平行于传感器表面,也可以垂直于传感器表面。平行方式相对优于垂直方式,当传感器上方不存在磁性微粒时,平行方式不会产生信号输出,而且激励场即使有一定的角度偏转,也不会导致片上分量的产生。另外,激励场可以采用直流激励场或交流激励场,在交流激励场作用下,传感器输出交流信号,通过锁相放大技术,可以获得较高的信噪比,方便信号的提取。但是,相比DC激励场而言,AC激励场会导致电磁干扰,需要在后端设计交流EMI滤波及整流滤波电路,增加了电路复杂性。另外,外加交流激励磁场频率需要均衡考虑,如果过高,系统中的感性阻抗元件(如电磁铁等)会使电桥输出的信号大幅减弱;如果激励磁场频率太低,又会增加1/f噪声。对于某些GMR传感器,还需要外加偏置磁场,用于固定自由层、控制传感器工作在线性区间以及防止磁性微粒的初始极化。然而亚微米级的传感器,由于其自由层已处于单磁畴状态,可以不施加偏置场,从而提高自由层磁化时的自由度,增加传感器在易轴的敏感性。
3.5采用信号放大技术
由于GMR传感器阵列输出的信号非常微弱,并且信号中不可避免地存在1/f噪声和散粒噪声,为了精确测量掩埋在噪声中生物信号的幅值及相位,通常用前置低噪声放大器、带通滤波器、可控增益放大器、相敏检测电路、正交移相电路、差分直流放大电路等组成的锁相放大设备来抑制差模噪声和共模噪声,对传感器输出的信号进行预处理。
4结语
利用GMR传感器组成阵列,对磁性标记的生物分子的检测进行研究工作已经开展了近十年,这里就检测方法的基本原理、发展情况、影响检测效果的各项因素进行介绍和分析。目前制约GMR传感器阵列生物检测性能的关键是制备工艺和材料的问题,在进一步的研究中,需要采用生物分子尺度相同、高灵敏的新型GMR传感器,研究新的生物机能性保护膜,在避免互扰的基础上,在芯片上布局更密集、有效生物结合面更大的阵列,改善传感器的线性度,保证亚微米级的超顺磁颗粒形态的均一,才能有效促进GMR优越感器阵列在生物检测上的应用。
欢迎分享,转载请注明来源:内存溢出

 微信扫一扫
微信扫一扫
 支付宝扫一扫
支付宝扫一扫
评论列表(0条)