
1 前言
盐雾试验是集成电路可靠性试验之一,它可以用来检验产品的抗腐蚀环境能力的强弱。而盐雾试验所需的条件又比较多,这些条件会对试验产生一定的影响。
2 试验
一般我们做盐雾试验的条件是盐液:NaCl(无水);pH值:6.5~7.2;温度:32-38℃;盐雾沉积率:20000~50000/m2 (24h);盐雾持续时间:24h,48h,96h,240h;盐浓度:0.5%-3%。
盐雾沉积率与盐浓度是相对应的,这是因为它们之间的对应关系如下式
Sd为盐雾沉积率;[Cl]-为氯离子浓度。
因为盐浓度就是氯离子浓度,所以盐浓度与盐雾沉积率之间是相对应的。
根据以上条件可以判断,在进行盐雾试验时,影响试验的主要条件有以下几点:温度;盐液浓度;氧的溶解度;流速。
为了验证以上的条件对试验的影响,本文选用若干表面干净的电路按下列方法进行试验验证。
方法1:盐选用NaCl(无水);温度为35℃;时间为24h。流速一定;按盐浓度为1%,2%,3%,4%,5%分五组进行试验,每一组五个电路。
方法2:盐选用NaCl(无水);浓度为3%;盐雾沉积率为50000/m2*24h;时间为24h。流速一定;按温度20℃,25℃,30℃,35℃,40℃,50℃分六组进行试验,每一组五个电路。
方法3:盐选用NaCl(无水);浓度为3%;盐雾沉积率为50000/m2(24h);时间为24h。温度为35℃;按流速正常和流速变大分两组进行试验,每一组五个电路。
另外,为了研究样品的摆放对试验的影响,我们用方法4进行试验。
方法4:将15只样品平均分成三组,盖板向上,样品偏离垂直方向30°,45°,75°,90°进行试验,其他试验条件是:盐选用NaCl(无水);浓度为3%;盐雾沉积率为:50000/m2(24h);时间为24h。流速一定;温度为35℃。
试验后用纯净水清洗电路,放置1小时后,试验结果见表1。
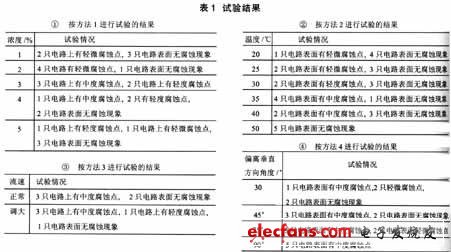
3 试验分析
本文对以上试验结果进行了分析。在盐雾试验中,由于各种金属的电极电位不同以及它们在盐液中的过电位大小不一,所以在盐雾中会发生很多的 电化学反应。在阳极是金属失去电子,成为离子,在阴极发生的电化学反应类型有析氢反应和氧去极化反应等,其中氧去极化反应(吸氧反应)是最主要的反应类型。它是由于盐液中含有的溶解氧而 造成的,溶液中的氧可通过扩散作用不断地向阴极区移动。
氧向电极表面扩散决定整个吸氧腐蚀过程的速度,因为氧在盐溶液的溶解度是有限的,吸氧腐蚀速度往往被氧向金属表面的扩散速度所控制,也就是说,金属腐蚀速度是与氧在阴极还原的极限电流密度相一致的。
氧向阴极扩散速度由Fick第二定律得出
式中,D为溶解氧扩散系数;δ为扩散层厚度;Ce为电极表面氧的浓度;C为溶液中氧的浓度。
电极反应速度可由法拉第定律得出
id:极限电流密度;n:价数;F:法拉第常数。
当电极反应达到平衡,即扩散控制时:V1=V2由公式(2)、公式(3)得出
由于随着电极反应的进行,电极附近氧原子不断消耗,Ce降低,当Ce→0时,公式(4)可变为
从公式(5)中可以看出,极限电流密度id与扩散层厚度δ、溶解氧扩散系数D、溶解氧的浓度C、价数n等有关;极限电流密度的大小也就意味着腐蚀速度的大小;其中D与环境温度成正比。
欢迎分享,转载请注明来源:内存溢出

 微信扫一扫
微信扫一扫
 支付宝扫一扫
支付宝扫一扫
评论列表(0条)