
早在1801年,一位名名叫Nicolas Gautherot法国科学家观察到,在电解测试中,即使主电池断开,也存在极少量的电流。而在1859年,一位名名叫Gatson的科学家开发了铅酸电池,这是第一个通过反向电流进行充电的电池。
这是铅酸电池的最初版本,后来Camille Alphonse Faure随后对其进行了许多改进。最终,亨利·都铎(Henri Tudor)于1886年发明了实用型铅酸电池。为此,本文简单来介绍下铅酸电池的结构、工作原理和主要类型。
基本结构
铅酸电池属于可充电电池和二次电池的分类,尽管电池的能量与体积、能量与重量的比例最小,但铅酸电池具有提供增加的浪涌电流的能力。这对应于铅酸电池具有大量的功率重量比。
这些是利用过氧化铅和海绵铅将化学能转化为电能的电池。这些主要用于变电站和电力系统,因为它们提高了电池电压水平和最低成本。
在铅酸电池结构中,极柱和容器是关键部件。下面简单说明下每个组件的详细功能,其结构图如下所示:
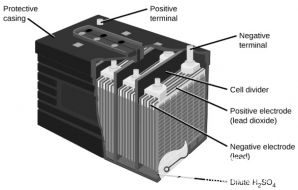
1、容器
容器部件由硬橡胶、铅涂层木材、玻璃、由沥青元素制成的硬橡胶、陶瓷材料或锻造塑料制成,它们放置在顶部以消除任何类型的电解液放电。而在容器底部,有四个肋拱,其中两个放置在正极板上,另量个放置在负极板上。
另外,棱镜充当两个板的底座,此外它还保护板免受短路。用于制造容器的部件应不含硫酸,也不应弯曲或渗透,而且还要不含有任何会导致电解质损坏的杂质。
2、极柱
铅酸电池中的极柱以不同的方式构造,并且都由类似类型的网格组成,该网格由活性成分和铅构成。网格对于建立电流的导电性和将等量的电流传播到主动组件至关重要。如果分布不均匀,那么主动元件就会松动。
铅酸电池中的极板有两种形式,分别是植物板/成型板和浮雕板/粘贴板。
成型板主要用于静态电池,重量大,价格昂贵。但它们具有较长的耐用性,即使在连续充电和放电过程中也不易失去活性成分,并且具有最小的重量比例。
粘贴工艺板多用于制作负极板,而不是正极板。负极主动元件有些复杂,它们在充电和放电过程中经历了轻微的修改。
3、主动组件
主要在充电和放电时积极参与电池中发生的化学反应过程的成分称为主动组件,包括:
过氧化铅——形成一种正极主动组件。
海绵铅——这种材料形成了负极主动组件。
稀硫酸——主要用作电解质。
4、隔板
这些是由多孔橡胶、涂层铅木和玻璃纤维制成的薄片。隔板位于极柱之间以提供主动绝缘。它们的一侧具有凹槽形状,而其他边缘则具有光滑的饰面。
5、电池边缘
它具有直径为17.5毫米和16毫米的正边缘和负边缘。
工作原理
由于硫酸在电池中用作电解质,当它溶解时,其中的分子以SO4 –(负离子)和2H+(正离子)的形式分散,它们将自由运动。当这些电极浸入溶液中并提供直流电源时,正离子将发生运动并朝着电池负边缘的方向移动。同理,负离子也会有运动,朝着电池正边的方向移动。
每个氢离子和硫酸根离子从阴极和阳极收集一个和两个电子和负离子,它们与水发生反应。生成氢气和硫酸。而由上述反应产生的产物与氧化铅反应并形成过氧化铅。这意味着在充电过程中;铅阴极元件本身保持为铅,而铅阳极形成为深棕色的过氧化铅。
当没有直流电源时,如果在电极之间使用电压表连接时,它会显示电极之间的电位差。当电极之间有导线连接时,电流将通过外部电路从负极板流向正极板,这意味着电池具有提供电能形式的能力。
主要类型
铅酸电池类型主要分为五种,下面依次介绍下。
1、满液式——这是传统的发动机点火式,具有牵引式电池。电解液在电池部分自由移动。使用这种类型的人可以访问每个电池,当电池干涸时,他们可以向电池加水。
2、密封型——这种铅酸电池只是对浸没型电池的一个小改动。尽管人们无法接触到电池中的每个电池,但内部设计几乎与淹没型电池相似。这种类型的主要变化是存在足够量的酸来承受整个电池寿命期间化学反应的平稳流动。
3、VRLA型——这些被称为阀控式铅酸电池,也称为密封型电池。数值控制程序允许在充电时安全释放O2和H2气体。
4、AGM型——这是一种吸收玻璃磨砂型电池,允许电解液在极板材料附近停止。这种电池增强了放电和充电过程的性能。这些特别适用于动力运动和发动机启动应用。
5、凝胶型——这是一种湿式铅酸电池,其中该电池中的电解质与二氧化硅有关,这会使材料变硬。与其他类型的电池相比,电池的充电电压值最小,并且它也具有更高的灵敏度。
化学反应
电池中的化学反应主要发生在放电和再充电过程中。当电池完全放电后,正负极分别为PbO2和Pb。当这些使用电阻连接时,电池会放电,并且电子在充电时具有相反的路径。H2离子向阳极移动并成为原子。它与PbO2接触,从而形成白色的PbSO4 。
同样,硫酸根离子向阴极移动,到达后形成SO4。它与铅阴极反应,从而形成硫酸铅。其化学式如下:
PbSO4 + 2H = PbO + H2O
PbO + H2SO4 = PbSO4 + 2H2O
PbO2 + H2SO4 + 2H = PbSO4 + 2H2O
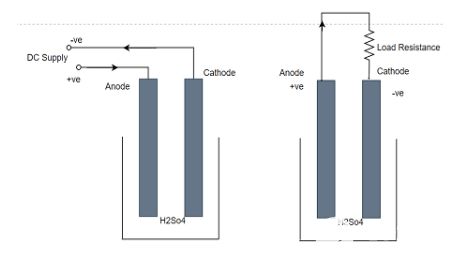
在再充电过程中,阴极和阳极与直流电源的负边沿和正边沿相连。正H2离子向阴极方向移动,它们获得两个电子并形成H2原子。它与硫酸铅发生化学反应,生成铅和硫酸。
PbSO4 + 2H2O + 2H = PbSO4 + 2H2SO4
两个过程的组合方程表示如下图所示:

注意:这里向下的箭头表示放电,向上的箭头表示充电过程。
生命周期
铅酸电池的最佳功能温度为25°C,即77°F。温度范围的增加会缩短使用寿命。根据规则,温度每升高80°C,电池的半衰期就会缩短。而在25°C下工作时铅酸电池寿命为10年。而当在33°C下运行时,它的寿命只有5年。
主要应用
铅酸电池的应用非常的广泛,下面简单列举一部分,如下:
用于应急照明,为污水泵提供电力。
用于电动机。
潜艇。
核潜艇。
总结
铅酸电池是一种电极主要由铅及其氧化物制成,电解液是硫酸溶液的蓄电池。它具有价格便宜、组成简单、再生利用、性能稳定、安全稳定等优势特点,因而被广泛的应用。
欢迎分享,转载请注明来源:内存溢出

 微信扫一扫
微信扫一扫
 支付宝扫一扫
支付宝扫一扫
评论列表(0条)