
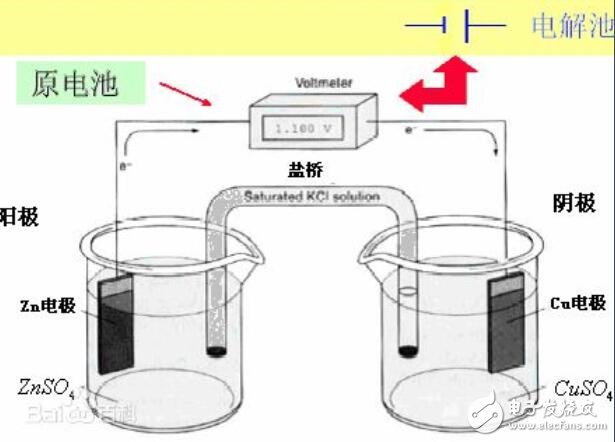
通过氧化还原反应而产生电流的装置称为原电池,也可以说是把化学能转变成电能的装置。有的原电池可以构成可逆电池,有的原电池则不属于可逆电池。原电池放电时,负极发生氧化反应,正极发生还原反应。例如铜锌原电池又称丹聂尔电池,其正极是铜极,浸中硫酸铜溶液中;负极是锌板,浸在硫酸锌溶液中。两种电解质溶液用盐桥勾通,两极用导线相连就组成原电池。平时使用的干电池,是根据原电池原理制成的。
原电池的发明历史可追溯到18世纪末期,当时意大利生物学家伽伐尼正在进行著名的青蛙实验,当用金属手术刀接触蛙腿时,发现蛙腿会抽搐。大名鼎鼎的伏特认为这是金属与蛙腿组织液(电解质溶液)之间产生的电流刺激造成的。1800年,伏特据此设计出了被称为伏打电堆的装置,锌为负极,银为正极,用盐水作电解质溶液。1836年,丹尼尔发明了世界上第一个实用电池,并用于早期铁路信号灯。
电解池的主要应用用于工业制纯度高的金属,是将电能转化为化学能的一个装置(构成:外加电源,电解质溶液,阴阳电极)。使电流通过电解质溶液或熔融电解质而在阴,阳两极引起还原氧化反应的过程。使电流通过电解质溶液或熔融的电解质而在阴、阳两极上引起还原氧化反应的过程叫做电解。把电能转变为化学能的装置叫做电解池或电解槽。当离子到达电极时,失去或获得电子,发生氧化还原反应的过程电解原理。是消耗电能的。
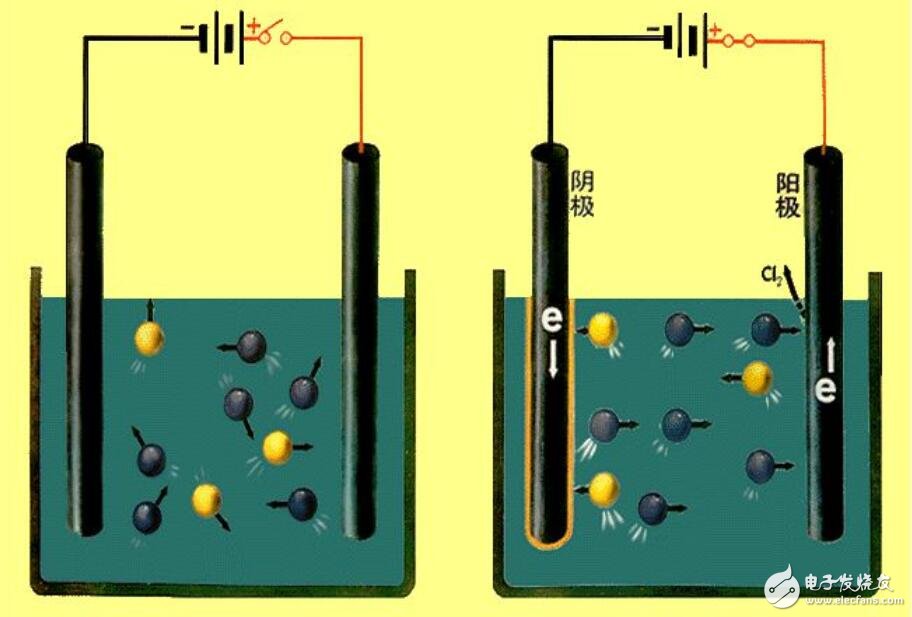
1、电解池与原电池的本质区别:电解池是把电能转化为化学能;原电池是把化学能转化为电能。
2、电解池与原电池装置的区别:电解池有外加电源;原电池没有外加电源。
3、电解池与原电池电子流向的区别:原电池的电子流向刚好跟电流的方向相反(电流正电荷流向,电子带负电);电解池刚好跟原电池的电子流向相反(电子经负极流出到电解池中)。
4、电解池与原电池的应用区别:原电池应用在铅蓄电池;电解池应用在电镀,精炼,冶金方面。
5、电解池与原电池级的区别:电解池叫阴阳极;原电池叫正负极。
6、电解池与原电池电的区别:原电池是对外供电,是自发的;电解池是需要通电,是被动的。
推荐阅读:
原电池的工作原理
原电池正负极的判断方法
欢迎分享,转载请注明来源:内存溢出

 微信扫一扫
微信扫一扫
 支付宝扫一扫
支付宝扫一扫
评论列表(0条)